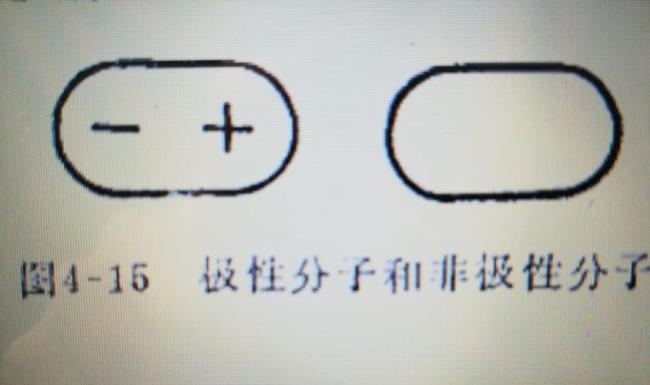
在化合物分子中,不同种原子形成的共价键,由于两个原子吸引电子的能力不同,共用电子必然偏向吸引电子能力较强的原子一方,因而吸引电子能力较弱的原子一方相对的显正电性,这样的共价键叫做极性共价键,简称极性键。非极性键:同种元素的原子形成的共价键,共用电子不偏移,显电中性。
并不是只有非金属元素之间才有可能形成极性共价键,金属与非金属之间也可以形成极性共价键(比如AlCl3,BeCl2等),一般来说,只要两个非金属原子间的电负性不同,且差距小于1.7,则形成极性键,大于1.7时,则形成离子键。
附注:极性键介于离子键和非极性键之间。
含有极性键的分子未必是极性分子,衡量极性分子的标准为偶极距的大小,只有当偶极距不为零时,分子才具有极性。
简单来说,分子中,中心原子化合价的绝对值<>原子最外层电子数时,为极性分子。
以下为常见的极性分子:
极性分子:HX(x为卤族元素),CO,NO,H2O,H2S,NO2,SO2,SCl2,NH3,H2O2,CH3Cl,CH2Cl2,CHCl3,CH3CH2OH
极性分子
如果分子的构型不对称,则分子为极性分子(polar molecules)。如:氨气分子,HCl分子等。区分极性分子和非极性分子的方法:非极性分子的判据:中心原子化合价法和受力分析法