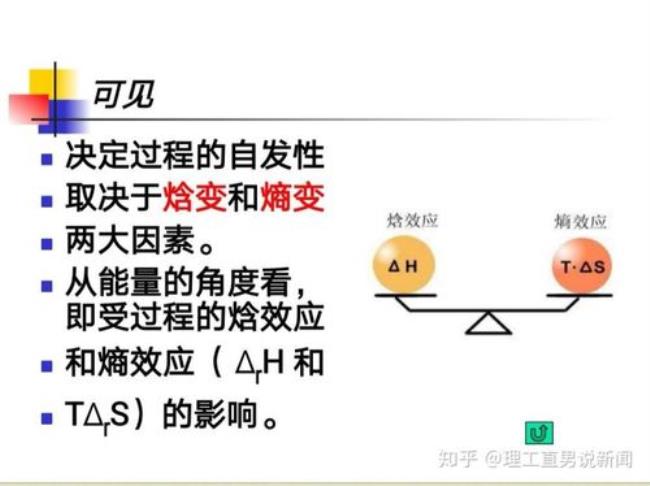
能量判据和熵判据的应用:
1、由能量判据知∶放热过程(△H﹤0)常常是容易自发进行
2、由熵判据知∶许多熵增加(△S﹥0)的过程是自发的
3、很多情况下,简单地只用其中一个判据去判断同一个反应,可能会出现相反的判断结果,所以我们应两个判据兼顾。由能量判据(以焓变为基础)和熵判据组合成的复合判据将更适合于所有的反应过程
4、过程的自发性只能用于判断过程的方向,不能确定过程是否一定会发生和过程的速率
5、在讨论过程的方向时,我们指的是没有外界干扰时体系的性质。如果允许外界对体系施加某种作用,就可能出现相反的结果
6、反应的自发性也受外界条件的影响
(1)向上抛一小球,然后让小球在地面上反复弹起,由于多种
原因,小球每次弹起的高度都比前一次低,最后停止在地面上,但
地面上停止的小球不会自动弹起,宏观上具有不可逆性。
(2)理想气体向真空膨胀。
(3)浓度不等的溶液混合均匀。
(4)热量自发地由高温物体传向低温物体,直至两物体温度
相等,推动力为温度差。
(5)水从高处流向低处,如瀑布。
说明自发过程一旦发生,总是沿单方向进行,达到一定程度
即平衡时停止变化,而它们的逆过程则一定不能自动发生