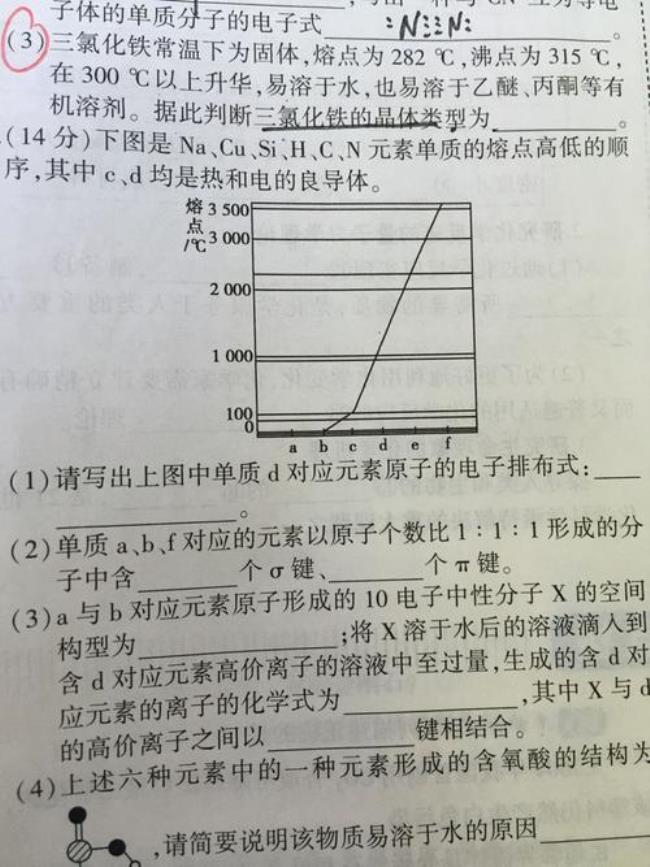
物质熔沸点高低的比较
1、分子晶体中组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点越高。
2、不同晶型的物质的熔沸点高低顺序一般是:原子晶体>离子晶体>金属晶体>分子晶体。
相同条件不同状态物质的熔沸点:
一、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。
二、不同类型晶体的比较规律:
一般来说,不同类型晶体的熔、沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔、沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。
原子晶体间靠共价键结合,一般熔、沸点最高离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高分子晶体分子间靠范德华力结合,一般熔、沸点较低金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高有低。例如:金刚石>食盐>干冰
三、同种类型晶体的比较规律
1、原子晶体:
熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大,熔沸点越高。
例如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
2、离子晶体:
熔、沸点的高低,取决于离子键的强弱。一般来说,离子半径越小,离子所带电荷越多,离子键就越强,熔、沸点就越高。
例如:MgO>CaO,NaF>NaCl>NaBr>NaI。
3、分子晶体:
熔、沸点的高低,取决于分子间作用力的大小。一般来说,组成和结构相似的物质,其分子量越大,分子间作用力越强,熔沸点就越高。
例如:F2