蛋白激酶 A (protein kinase A,PKA)又称依赖于cAMP的蛋白激酶A (cyclic-AMP dependent protein kinase A),是一种结构最简单、生化特性最清楚的蛋白激酶。
PKA全酶分子是由四个亚基组成的四聚体, 其中两个是调节亚基(regulatory subunit, 简称R 亚基),另两个是催化亚基(catalytic subunit, 简称 C 亚基)。R亚基的相对分子质量为49~55kDa, C亚基的相对分子质量为40kDa,总相对分子质量约为180kDa全酶没有活性。在大多数哺乳类细胞中,至少有两类蛋白激酶A, 一类存在于胞质溶胶,另一类结合在质膜、核膜和微管上。
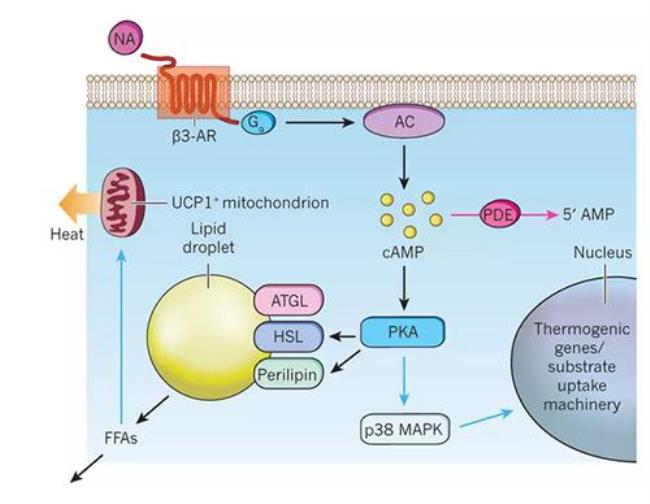
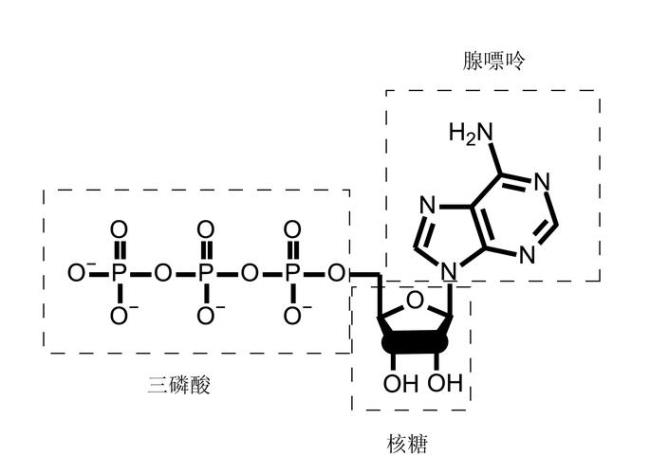
激酶是激发底物磷酸化的酶,所以蛋白激酶A的功能是将ATP上的磷酸基团转移到特定蛋白质的丝氨酸或苏氨酸残基上进行磷酸化, 被蛋白激酶磷酸化了的蛋白质可以调节靶蛋白的活性。
一般认为, 真核细胞内几乎所有的cAMP的作用都是通过活化PKA,从而使其底物蛋白发生磷酸化而实现的。
蛋白激酶A(Protein Kinase A,PKA):由两个催化亚基和两个调节亚基组成(图8-15),在没有cAMP时,以钝化复合体形式存在。cAMP与调节亚基结合,改变调节亚基构象,使调节亚基和催化亚基解离,释放出催化亚基。活化的蛋白激酶A催化亚基可使细胞内某些蛋白的丝氨酸或苏氨酸残基磷酸化,于是改变这些蛋白的活性,进一步影响到相关基因的表达。
蛋白激酶A在细胞中具有多种功能,包括调节糖原、糖和脂质的代谢。