电荷守恒:
c(Na+) + c(H+) == c(OH-) + c(HCO3-)
原则是:正电荷数等于负电荷数(注意如果不是一价的,例如二价则需乘以2)
物料守恒:
c(Na+) == C( HCO3-) + c(CO32-) + c(H2CO3)
原则是:钠元素与碳元素是1:1,如果是碳酸钠则该式为c(Na+) == 2{C( HCO3-) + c(CO32-) + c(H2CO3)}即钠元素与碳元素是2:1
电荷守恒:{Na+}+{H+}=2{CO32-}+{HCO3-}+{OH-}
物料守恒:{Na+}={H2CO3}+{CO32-}+{HCO3-}
电离:
H2O ==(可逆符号) H+ + OH-
NaHCO3 == Na+ + HCO3-
水解:
HCO3 + H2O ==(可逆符号) H2CO3 + OH-
电荷守恒:
{Na+} + {H+} == {OH-} + {HCO3-}
物料守恒:
C Na+ == C HCO3- == {HCO3-} + {H2CO3}
水解方程式:clo- + h2o <--> hclo + oh-
浓度大小:c(na+) > c(clo-) > c(oh-) > c(h+)
电荷守恒:c(na+) + c(h+) = c(clo-) + c(oh-)
物料守恒:c(na+) = c(clo-) + c(hclo)
质子守恒:c(h+) + c(hclo) = c(oh-)
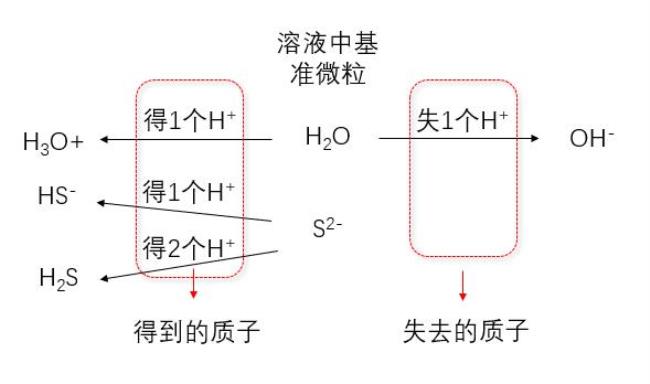
na2s
水解方程式:s2- + h2o <--> hs- + oh-
浓度大小:c(na+) > c(s2-) > c(oh-) > c(hs-) > c(h+)
电荷守恒:c(na+) + c(h+) = 2*c(s2-) + c(hs-) + c(oh-)
物料守恒:c(na+) = 2*[c(s2-) + c(hs-) + c(h2s)]
质子守恒:c(h+) + c(hs-) + 2*c(h2s) = c(oh-)
na2so3
水解方程式:so3^2- + h2o <--> hso3- + oh-
浓度大小:c(na+) > c(so3^2-) > c(oh-) > c(hso3-) > c(h+)
电荷守恒:c(na+) + c(h+) = 2*c(so3^2-) + c(hso3-) + c(oh-)
物料守恒:c(na+) = 2*[c(so3^2-) + c(hso3-) + c(h2so3)]
质子守恒:c(h+) + c(hso3-) + 2*c(h2so3) = c(oh-)