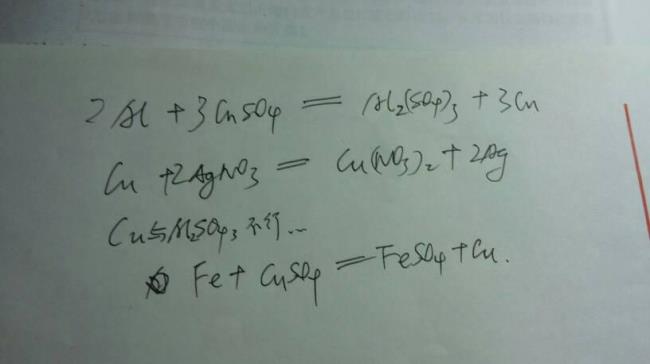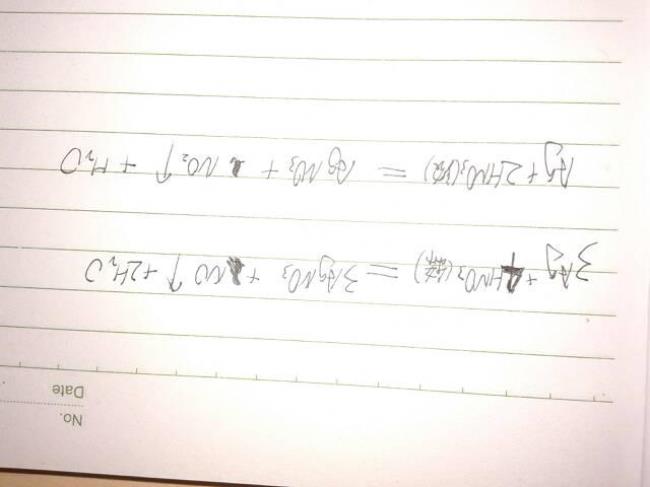Cu 由0价升为+2价,HNO3中的N由+5降为NO中的+2价
2-0=2,5-2=3,2和3的最小公倍数为6
那么Cu前写上3,NO前写上2(不在HNO3前写上2是因为有一部分的HNO3中的N没有改变化合价。即HNO3在这个反应里一部分充当酸,一部分充当氧化剂)
然后Cu(NO3)2之前也要写上3(Cu守恒)
然后,计算右边的N有8个,那就在左边的HNO3前写上8
最后计算左边的H或者O(显然H较简单),H有8个,那么右边H2O前就写上4
完成:3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ + 4H2O
总结:氧化还原反应的方程式一般先找到氧化元素和还原元素,然后先把二者配平了,再考虑其他的,H20一般最后考虑。